固有免疫應答(dá)是宿主識别與抵抗病原體感染的第一道(dào)防線,對(duì)激活适應性免疫進而清除病原體至關重要。位于細胞膜表面、内體或細胞質的模式識别受體(pattern recognition receptor,PRRs)通過識别病原體相關分子模式(pathogen-associated molecular patterns,PAMPs)或宿主損傷相關分子模式(damageassociated molecular patterns,DAMPs)啓動固有免疫應答(dá)抑制病原體的感染。作(zuò)爲固有免疫的重要組成部分,細胞焦亡是一種由 Gasdermin (GSDM)家族蛋白(bái)活化介導的新型程序性細胞死亡,在清除内源病變或外(wài)源感染過程中發揮關鍵作(zuò)用(yòng)。
什(shén)麽是細胞焦亡
細胞焦亡是一種由Gasdermin家族蛋白(bái)介導的新型程序性細胞死亡。當宿主細胞感應病原體感染或其他(tā)危險信号時(shí),Gasdermin 家族蛋白(bái)被切割活化并誘導細胞焦亡。細胞焦亡過程往往伴随大(dà)量炎性細胞因子釋放(fàng),這(zhè)些(xiē)炎性細胞因子在宿主清除病原體過程中發揮着至關重要作(zuò)用(yòng)。
關鍵蛋白(bái)Gasdermin
Gasdermin家族包含六個成員: GSDMA 、GSDMB、GSDMC、GSDMD、GSDME(又稱 DFNA5)
和(hé)PJVK(又稱 DFNB59)。除PJVK外(wài),GSDMA-E均由功能(néng)保守的N端結構域(GSDM-NT)和(hé)C端結構域(GSDM-CT)組成。GSDM-NT能(néng)夠結合細胞膜酸性磷脂或線粒體心磷脂,并在膜上(shàng)多聚化形成孔洞以誘導細胞焦亡。大(dà)量研究結果顯示革蘭氏陰性菌主要通過激活炎症小(xiǎo)體(inflammasome)進而切割活化GSDMD以觸發細胞焦亡。
炎症小(xiǎo)體包括經典炎症小(xiǎo)體和(hé)費經典炎症小(xiǎo)體。經典炎症小(xiǎo)體主要由Caspase-1、胞質内的
模式識别受體(NLRP3、NLRC4、NLRP1、AIM2、Pyrin等)和(hé)凋亡相關斑點樣蛋白(bái)(Apoptosis-associated Speck-like Protein,ASC)組成。經典炎症小(xiǎo)體組裝後激活Caspase-1進而切割GSDMD,釋放(fàng)GSDMD-NT導緻細胞焦亡。與此同時(shí),Caspase-1切割活化IL-1β和(hé)白(bái)介素18(IL-18)等促炎症因子,招募免疫細胞,清除外(wài)源病原體或内源病變。
非經典炎症小(xiǎo)體由病原菌感染條件下(xià)釋放(fàng)脂多糖(lipopolysaccharide,LPS)至胞内直接結合并激活Caspase-4/5/11,活化的Caspase-4/5/11切割 GSDMD形成具有成孔活性的GSDMD-N 端結構域并誘導細胞焦亡。
近年來(lái),不依賴于炎症小(xiǎo)體介導的細胞焦亡通路的活化機制相繼報(bào)道(dào)。包括,細胞凋亡通路的執行蛋白(bái)Caspase-3能(néng)夠切割GSDME,釋放(fàng)GSDME-NT,促使細胞凋亡轉變爲細胞焦亡;GSDMD 能(néng)夠被中性粒細胞彈性蛋白(bái)酶(neutrophil elastase,ELANE)和(hé)組織蛋白(bái)酶G(cathepsin G,CatG)切割活化,引起細胞焦亡;殺傷細胞釋放(fàng)顆粒酶 B(granzyme B,GZMB)直接切割腫瘤細胞GSDME觸發腫瘤細胞焦亡;耶爾森菌(Yersinia)分泌的外(wài)膜蛋白(bái)J(Yersinia outer protein J,YopJ)抑制轉化生長因子β激活激酶 1 (transforming growth factor-β-activated Kinase 1,TAK1),激活RIPK1/Caspase-8複合體,活化的Caspase-8切割GSDMD導緻細胞焦亡;族鏈球菌(Group A Streptococcus,GAS)感染過程中釋放(fàng)的效應蛋白(bái)鏈球菌熱源性外(wài)毒素B (Streptococcal pyrogenic exotoxin B,SpeB),一種胱氨酸蛋白(bái)酶,直接剪切宿主GSDMA誘導細胞焦亡等等。這(zhè)些(xiē)研究進一步拓展和(hé)突出了(le)細胞焦亡在抗感染和(hé)抗腫瘤領域的功能(néng)。
病原體抑制細胞焦亡的新策略
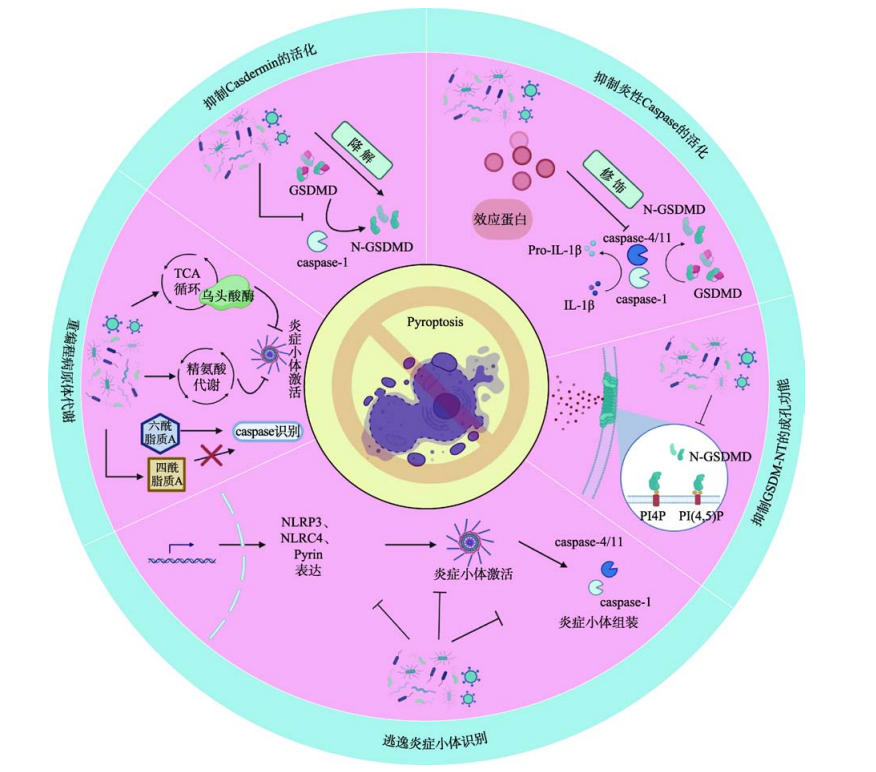
Novel strategies for pyroptosis suppression by pathogen
病原體在與宿主長期“博弈”過程中進化出多種抑制細胞焦亡的策略,主要包括:
(1) 逃逸炎症小(xiǎo)體識别;
病原體可從(cóng)抑制模式識别受體激活和(hé)表達、抑制炎症小(xiǎo)體組裝等方面逃逸宿主炎症小(xiǎo)體識别。幹擾宿主炎症小(xiǎo)體對(duì)病原體的識别已經成爲細菌發生免疫逃逸的新策略,對(duì)于增強細菌的毒力并建立有效的感染至關重要。
(2) 重編程病原體自(zì)身代謝(xiè)抑制炎症小(xiǎo)體活化;
巨噬細胞 (macrohages) 是免疫系統中的重要細胞,能(néng)夠吞噬和(hé)消滅病原體,巨噬細胞表面的酪氨酸激酶受體VEGFR3與AMPK形成的信号軸能(néng)整合糖代謝(xiè)、炎症小(xiǎo)體活化、細胞焦亡和(hé)吞噬清除細菌的功能(néng)。
(3) 分泌效應蛋白(bái)抑制炎性 Caspase的活性;
病原體分泌的效應蛋白(bái)能(néng)夠直接與Caspase相互作(zuò)用(yòng)并抑制其活性從(cóng)而阻斷炎症小(xiǎo)體介導的細胞焦亡。
(4) 抑制Gasdermin的活化;
Gasdermin 家族蛋白(bái)是細胞焦亡的關鍵執行蛋白(bái),病原體可以直接抑制該家族蛋白(bái)的活性和(hé)表達而抑制細胞焦亡。
(5) 抑制GSDM-NT的成孔功能(néng)。
泛素化是一種能(néng)夠調節多種細胞功能(néng)的翻譯後修飾,由活化酶E1,結合酶E2 和(hé)連接酶E3 催化完成。泛素化不僅能(néng)夠靶向底物蛋白(bái)以26S蛋白(bái)酶體依賴的方式使其降解,還在調節先天性和(hé)适應性免疫反應以及免疫耐受方面具有關鍵作(zuò)用(yòng)。一些(xiē)病原體已進化出複雜(zá)的機制以逃避或抵消泛素依賴的宿主反應,其中由病原體編碼的 E3 泛素連接酶和(hé)去泛素化酶在病原體-宿主細胞相互作(zuò)用(yòng)中發揮至關重要的作(zuò)用(yòng)。
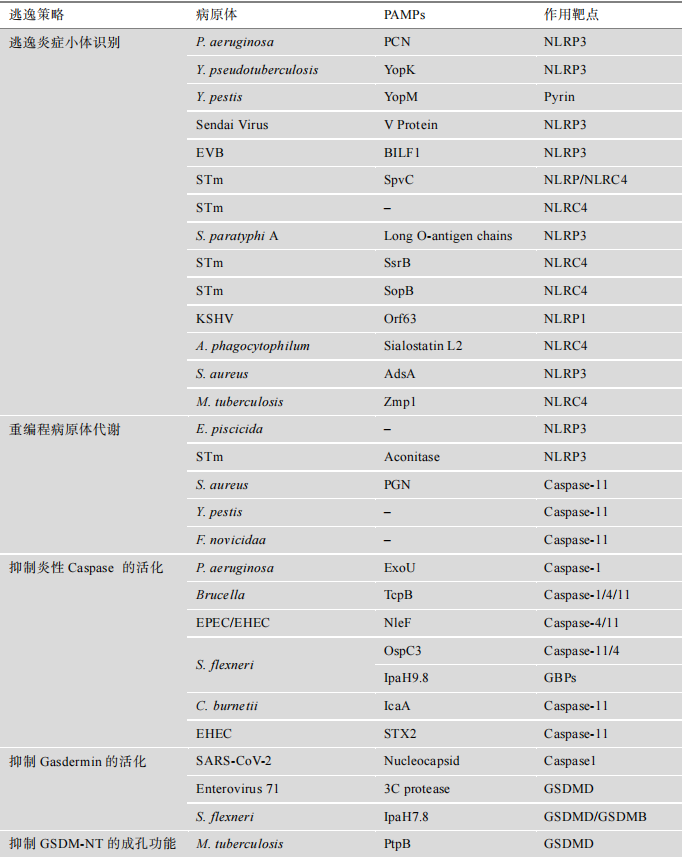
Novel strategies for pyroptosis suppression by pathogen
細胞焦亡是機體抵抗病原體感染的一種重要天然免疫反應,而病原體在宿主免疫系統的壓力下(xià)進化出了(le)适應性策略來(lái)抑制細胞焦亡以實現(xiàn)持續感染。病原體逃逸細胞焦亡的相關研究有助于進一步了(le)解病原體-宿主相互作(zuò)用(yòng)機制,爲開(kāi)發新型抗感染治療策略奠定了(le)重要理(lǐ)論基礎。

 聯系我們
聯系我們





