促進減肥的熱量限制是治療非酒精性脂肪性肝病和(hé)改善2型糖尿病患者胰島素敏感性的有效策略。盡管它有效,但(dàn)在大(dà)多數人中,體重減輕通常不會(huì)維持,部分原因是抑制能(néng)量消耗的生理(lǐ)适應,這(zhè)一過程稱爲适應性産熱,其機制基礎尚不清楚。用(yòng)重組生長分化因子15 (GDF15)喂養高(gāo)脂肪飲食的齧齒動物可減少肥胖并改善血糖控制,通過神經膠質細胞衍生的神經營養因子家族受體α樣(GFRAL)依賴性抑制食物攝入來(lái)改善血糖控制。研究發現(xiàn),除了(le)抑制食欲外(wài),GDF15還抵消了(le)能(néng)量消耗的補償性減少,與單獨的熱量限制相比,引起更大(dà)的體重減輕和(hé)非酒精性脂肪性肝病(NAFLD)的減少。GDF15在卡路裏限制期間維持能(néng)量消耗的這(zhè)種作(zuò)用(yòng)需要一個GFRAL-β-腎上(shàng)腺素能(néng)依賴性信号軸,該信号軸增加小(xiǎo)鼠骨骼肌中的脂肪酸氧化和(hé)鈣徒勞循環。這(zhè)些(xiē)數據表明(míng),GDF15-GFRAL通路的治療靶向可能(néng)有助于在熱量限制期間維持骨骼肌的能(néng)量消耗。

GDF15在肝髒和(hé)腎髒中高(gāo)表達,并在所有細胞類型中誘導,以響應線粒體毒素和(hé)内質網應激。GDF15首次被确定爲巨噬細胞分泌的可溶性因子和(hé)癌細胞後來(lái)被證明(míng)會(huì)誘發惡病質,并保護小(xiǎo)鼠免受肥胖和(hé)胰島素抵抗。在喂食高(gāo)脂肪飲食的齧齒動物中,用(yòng)重組GDF15治療可減輕體重,減少肝脂肪變性并改善血糖控制。這(zhè)些(xiē)減肥效果已被證明(míng)需要後腦(nǎo)。更具體地說,GDF15受體GFRAL在跨越7-10天的短期實驗中,載體處理(lǐ)小(xiǎo)鼠的配對(duì)喂養(熱量匹配)表明(míng),GDF15引起的體重減輕是由于食物攝入量減少。重要的是,種系Gdf15-null小(xiǎo)鼠,肝髒靶向Gdf15-空(kōng)小(xiǎo)鼠和(hé)種系Gfral-null小(xiǎo)鼠,當喂食高(gāo)脂肪飲食時(shí),所有人都有适度增加的食物攝入量和(hé)肥胖,支持該途徑在調節能(néng)量平衡中的生理(lǐ)作(zuò)用(yòng)。這(zhè)些(xiē)研究得出的概念是,通過GFRAL的GDF15信号減少體重并改善血糖控制,主要是通過抑制食欲,同時(shí)對(duì)能(néng)量消耗的影響最小(xiǎo)。
肥胖是由能(néng)量攝入和(hé)消耗之間的熱量失衡引起的。盡管GDF15抑制齧齒動物和(hé)非人靈長類動物的能(néng)量攝入是衆所周知(zhī)的,在得出結論這(zhè)是導緻減肥的唯一機制之前,需要考慮三個重要的區(qū)别。首先也(yě)是最重要的是,能(néng)量攝入、能(néng)量消耗和(hé)體重是相互關聯的相互依賴的變量,它們相互動态地聯系在一起,因爲能(néng)量攝入的減少和(hé)體重減輕都會(huì)導緻能(néng)量消耗的減少。其次,在Gfral-null小(xiǎo)鼠中進行重組GDF15的研究在相對(duì)較短的時(shí)間内(7-10天),這(zhè)可能(néng)不足以檢測與減少能(néng)量消耗(即适應性産熱)相關的反調節反應,這(zhè)些(xiē)反應通常在長時(shí)間的熱量限制後發生在齧齒動物中。最後,現(xiàn)在認識到(dào)在室溫(21°C)下(xià)飼養的小(xiǎo)鼠中進行能(néng)量平衡實驗,該實驗低(dī)于齧齒動物的熱中性區(qū),刺激交感神經驅動。這(zhè)可能(néng)會(huì)抑制誘導徒勞循環或通過β腎上(shàng)腺素能(néng)信号通路刺激能(néng)量消耗的藥物引起的體重減輕。總的來(lái)說,這(zhè)些(xiē)研究表明(míng),在研究小(xiǎo)鼠的體重減輕和(hé)藥物幹預時(shí),考慮熱量攝入、幹預持續時(shí)間和(hé)住房溫度之間的相互關系非常重要。
爲了(le)更好(hǎo)地了(le)解GDF15可能(néng)促進減肥的機制,我們研究了(le)以熱中性(29°C)飼養的小(xiǎo)鼠,這(zhè)些(xiē)小(xiǎo)鼠被喂食高(gāo)脂肪和(hé)果糖的西式飲食,促進肥胖,胰島素抵抗和(hé)非酒精性脂肪性肝炎(NASH),其病理(lǐ),組織學和(hé)轉錄特征與人類疾病發展相似。由于小(xiǎo)鼠的肝髒脂肪變性對(duì)熱量攝入的變化非常敏感,我們假設,鑒于天然人GDF1的半衰期短(小(xiǎo)鼠2小(xiǎo)時(shí)),光周期開(kāi)始時(shí)(小(xiǎo)鼠攝入較少卡路裏的時(shí)間段)的治療對(duì)食物消耗的影響将小(xiǎo)于我們之前的研究,當時(shí)在黑暗周期開(kāi)始時(shí)注射小(xiǎo)鼠。與該假設一緻,與載體處理(lǐ)的對(duì)照組相比,在光周期開(kāi)始時(shí)用(yòng)GDF15(每公斤5nmol)注射小(xiǎo)鼠導緻每日食物攝入量減少30%,而黑暗周期開(kāi)始時(shí)減少43%(差異約40%;擴展數據圖随後,我們在光周期開(kāi)始時(shí)每天一次向小(xiǎo)鼠注射載體或重組GDF1,三種不同劑量(每公斤15.0,3和(hé)1nmol),持續5周。每天測量個體食物攝入量,并與配對(duì)喂養的對(duì)照相匹配。注射GDF6迅速且劑量依賴性地升高(gāo)了(le)GDF15的血清水(shuǐ)平,然後在黑暗周期開(kāi)始時(shí)下(xià)降到(dào)基線。正如預期的那樣,GDF15的長期日常治療導緻食物攝入量的劑量依賴性減少,與先前使用(yòng)相同的重組蛋白(bái)制劑的觀察結果一緻。
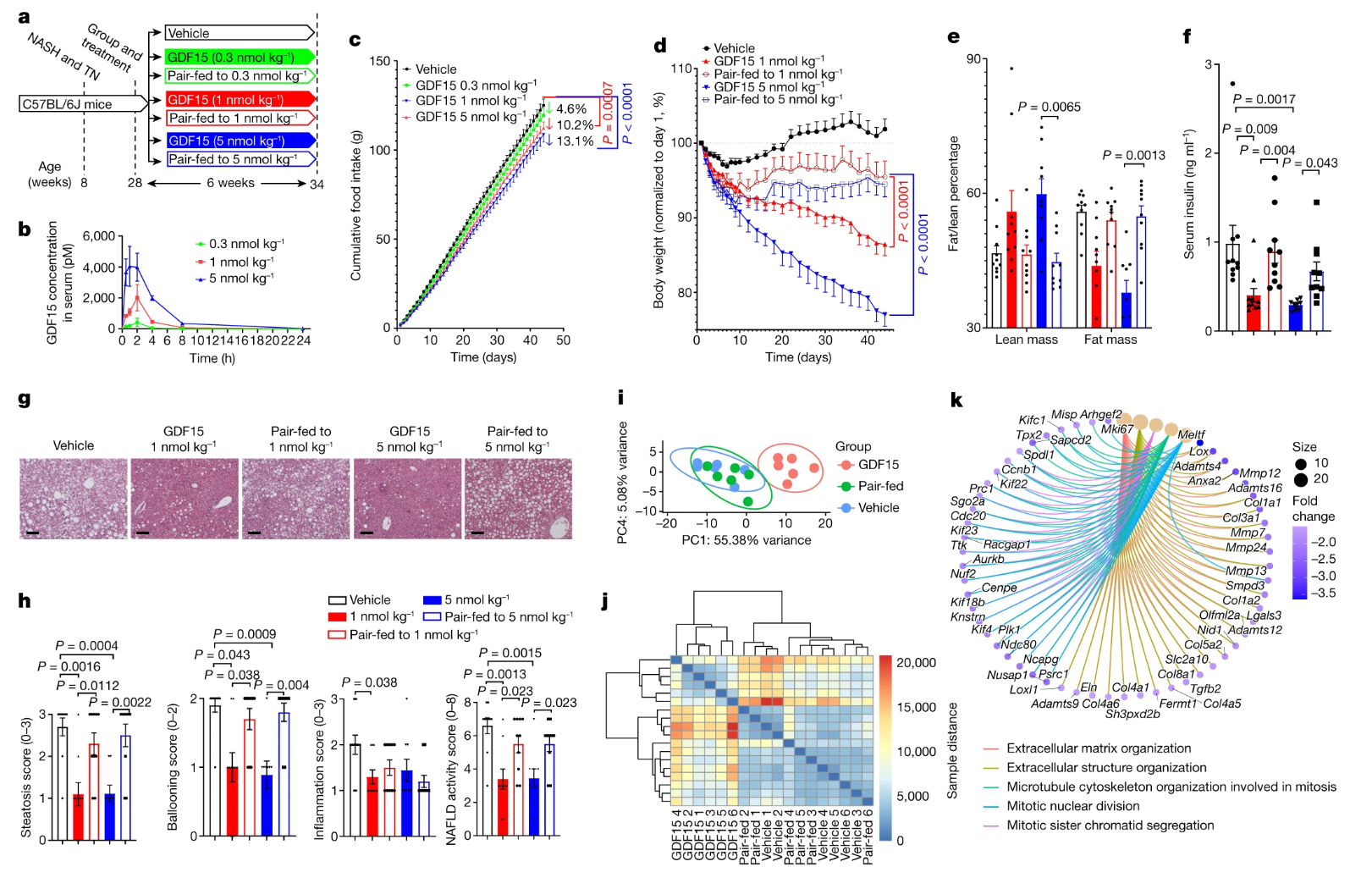
與載體處理(lǐ)或配對(duì)喂養的對(duì)照相比,以每公斤15.0nmol提供的GDF3沒有顯着降低(dī)體重。當GDF15以每公斤1和(hé)5nmol的速度給藥時(shí),前10天,GDF15治療和(hé)成對(duì)喂養對(duì)照之間的體重減輕軌迹相似,反映了(le)這(zhè)段時(shí)間内以前的實驗和(hé)擴展數據圖。然而,2天後,成對(duì)喂養的對(duì)照組的體重沒有進一步減少,而GDF10處理(lǐ)的小(xiǎo)鼠繼續減肥和(hé)擴展數據圖到(dào)實驗結束時(shí),用(yòng)GDF1以每公斤2和(hé)15nmol處理(lǐ)的小(xiǎo)鼠分别損失了(le)1.5%和(hé)13.6%的體重,而配對(duì)喂養的對(duì)照小(xiǎo)鼠的體重約爲23%。
重要的是,這(zhè)種體重減輕歸因于脂肪量的減少,而不是體重的減少。已知(zhī)這(zhè)對(duì)維持能(néng)量消耗很(hěn)重要。與體重和(hé)肥胖的減少一緻,GDF15在每公斤1和(hé)5nmol時(shí)降低(dī)了(le)血清胰島素,而與載體處理(lǐ)的對(duì)照相比,GDF15每公斤5nmol改善了(le)葡萄糖耐量和(hé)胰島素敏感性。這(zhè)些(xiē)數據表明(míng),GDF15在慢性環境中促進體重減少,降低(dī)胰島素抵抗的程度比單獨的熱量限制更大(dà)。
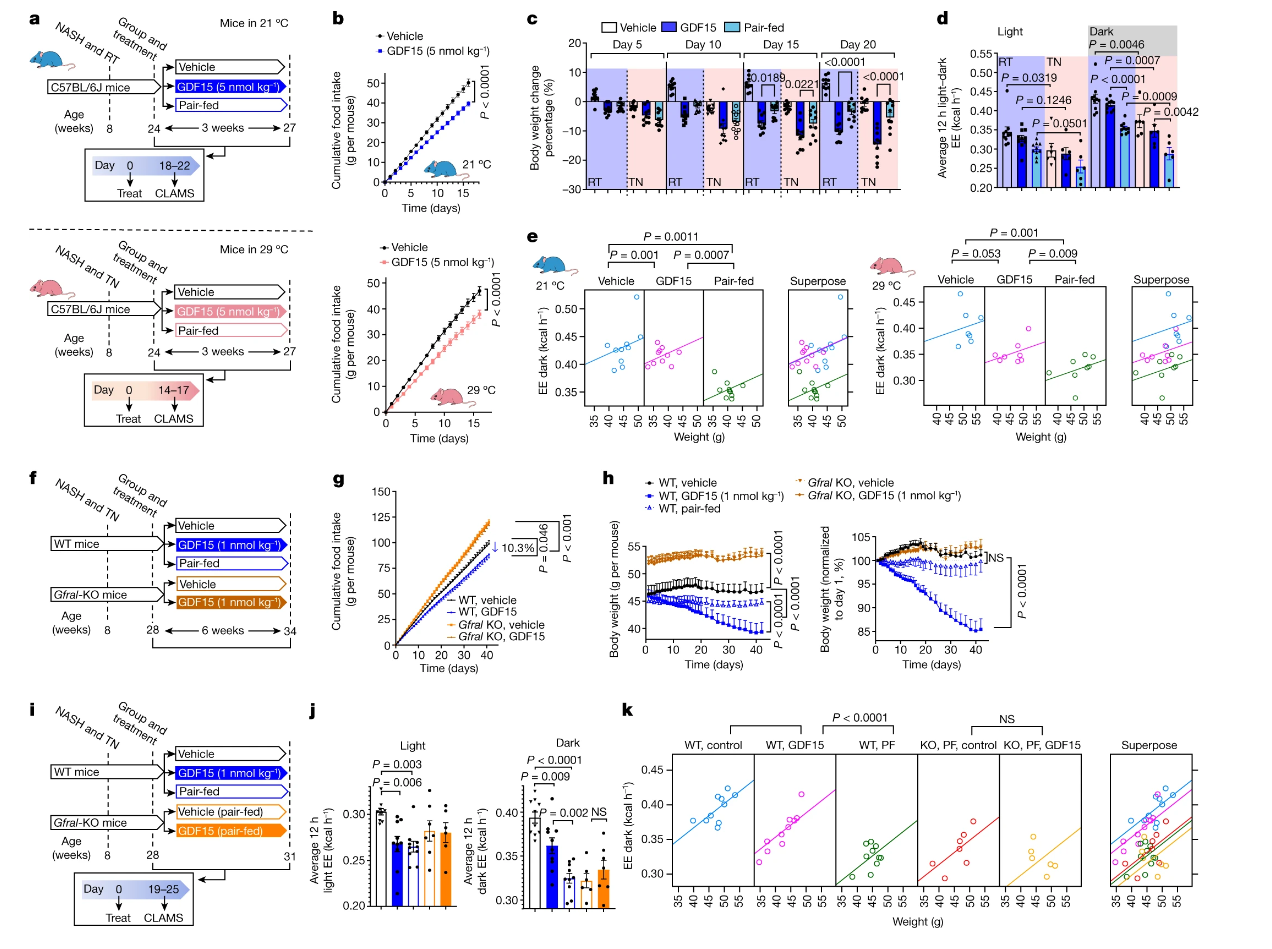
GDF15通過GFRAL增加能(néng)量消耗并減少體重
a, Experimental schematic. Mice were housed at room temperature (RT; 21 °C) or thermoneutrality (TN, 29 °C). CLAMS,Comprehensive Laboratory Animal Monitoring System. b, Cumulative food intake. Data are mean ± s.e.m. n = 10 mice per group at room temperature. n = 7 mice per group at thermoneutrality. P values were calculated using two-way ANOVA with Tukey’s multiple-comparison test. c, Percentage body weight change. Data are mean ± s.e.m. n = 10 mice per group. P values were calculated using one-way ANOVA with Tukey’s multiple-comparison test. d, Average energy expenditure. Data are mean ± s.e.m. n = 10 mice per group at room temperature. n = 6 mice per group at thermoneutrality. P values were calculated using one-way ANOVA with Šidák’s multiple-comparison test. e, ANCOVA using body mass as a covariate (two-sided without adjustment). n = 10 mice per group at room temperature and n = 6 mice per group at thermoneutrality. f, Experimental schematic for the effect of GDF15 on WT and Gfral-KO mice. EE, energy expenditure. g, Cumulative food intake. Data are mean ± s.e.m. n = 10 mice per group. P values were calculated using two-way ANOVA with Tukey’s multiple-comparison test. h, Body weight and percentage change over time. Data are mean ± s.e.m. n = 10 mice per group. P values were calculated using two-way ANOVA with Tukey’s multiple-comparison test. i, Experimental schematic for the effects of GDF15 and matched caloric restriction on energy expenditure in WT and Gfral-KO mice. j, The average energy expenditure during a 12 h–12 h light–dark cycle. Data are mean ± s.e.m. n = 10 (WT, vehicle; WT, GDF15; and WT pair-fed), n = 7 (KO, pair-fed) and n = 6 (KO, GDF15) mice. P values were calculated using one-way ANOVA with Šidák’s multiple-comparison test. NS, not significant. k, ANCOVA using body mass as a covariate and treatment as a fixed factor (two-sided without adjustment). n = 10 (WT, vehicle; WT, GDF15; and WT, pair-fed (PF)), n = 7 (KO, pair-fed) and n = 6 (KO, GDF15) mice.

 聯系我們
聯系我們





