傳統的基于抗體的靶向癌症治療是最有希望成功治療癌症的途徑之一,有可能(néng)減少對(duì)腫瘤細胞周圍健康細胞的毒副作(zuò)用(yòng)。然而,由于抗體體積大(dà)、穩定性低(dī)、清除緩慢和(hé)免疫原性高(gāo),抗體的全部潛力受到(dào)嚴重限制,因此開(kāi)發新型的、成功的癌症治療策略仍然具有挑戰性。
自(zì)1980年首次将單克隆抗體(monoclonal antibody,mAb)應用(yòng)于淋巴瘤患者以來(lái),具有高(gāo)度特異性的抗體已成爲癌症靶向治療和(hé)精準診斷的有力工(gōng)具。抗體(Abs)或免疫球蛋白(bái)(Igs)是天然衍生的治療性化合物,由脊椎動物免疫系統産生,用(yòng)于識别和(hé)消除外(wài)來(lái)病原體。抗體是150 kDa的蛋白(bái)質,由2條相同的重鏈和(hé)2條相同的輕鏈組成,它們通過二硫鍵和(hé)非共價相互作(zuò)用(yòng)連接在一起。一個抗體由2個抗原結合位點組成,每個抗原結合位點由2個可變結構域組成,分别稱爲VH和(hé)VL。
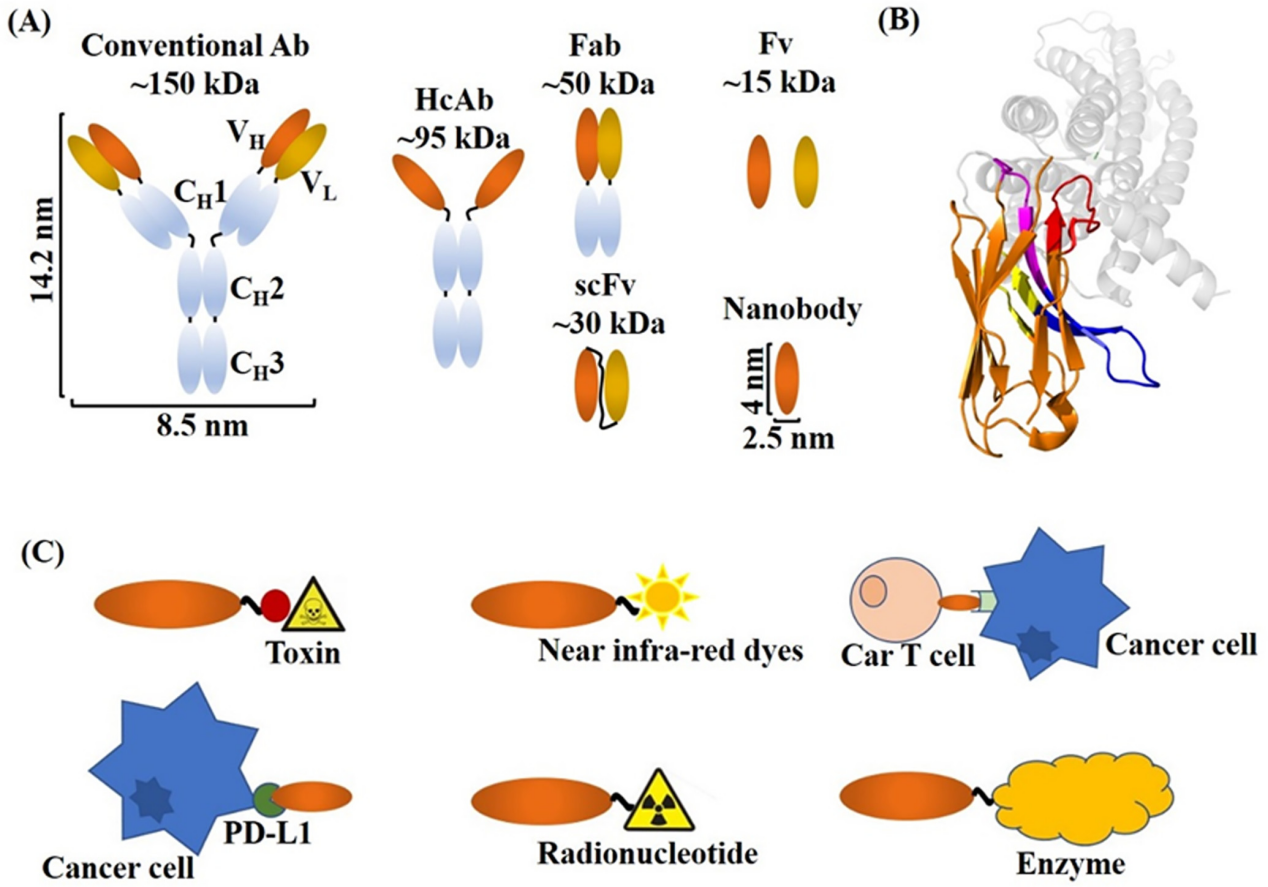
圖:Nb結構的描述及其在癌症治療和(hé)診斷中的應用(yòng)。(A)不同抗體的示意圖。傳統的抗體由兩條輕鏈和(hé)兩條重鏈組成。HcAb僅由兩條相同的重鏈組成。Nb是最小(xiǎo)的自(zì)然存在的抗原結合片段。(B) Nb結合其抗原G蛋白(bái)偶聯受體(GPCR)的晶體結構。GPCR爲灰色,FR區(qū)域(FR2除外(wài))爲橙色,FR2區(qū)域由特征親水(shuǐ)性氨基酸組成,CDR1、CDR2和(hé)延長的CDR3區(qū)域分别爲藍色、品紅(hóng)、黃色和(hé)紅(hóng)色(PDB ID: 4XT1)。(C) Nb偶聯物在癌症治療中的應用(yòng)示意圖。
抗體在癌症的臨床治療中已經應用(yòng)了(le)幾十年,到(dào)2021年,美(měi)國食品和(hé)藥物管理(lǐ)局已經批準了(le)79種治療性單克隆抗體,其中包括30種用(yòng)于治療癌症的單克隆抗體(monoclonal antibody,mAb)可直接與跨膜受體或可溶性配體結合,從(cóng)而幹擾腫瘤細胞中相應的信号通路。此外(wài),完整的抗體可以通過Fc功能(néng)域吸引NK細胞和(hé)巨噬細胞等效應細胞,引起抗體依賴性細胞介導的細胞毒性(ADCC)。此外(wài),抗體(Abs)已被用(yòng)作(zuò)靶向遞送細胞毒性藥物或含有治療分子的納米顆粒的載體。除了(le)靶向治療藥物外(wài),抗體還用(yòng)于臨床正電子發射斷層掃描(PET)、單光子發射計(jì)算(suàn)機斷層掃描(SPECT)或光學成像,在這(zhè)些(xiē)成像中,抗體可以将放(fàng)射性或熒光試劑引導到(dào)病變部位。然而,Abs的應用(yòng)受到(dào)限制,部分原因是由于其相對(duì)較大(dà)的尺寸(14.2 nm × 8.5 nm × 3.8 nm),如上(shàng)圖所示,這(zhè)被認爲是其不理(lǐ)想的藥代動力學特征和(hé)腫瘤穿透性有限的主要原因抗體的另一個複雜(zá)性來(lái)自(zì)于其複雜(zá)的結構,包括翻譯後的聚糖修飾和(hé)分子間和(hé)分子内的二硫鍵,導緻大(dà)規模生産抗體的成本很(hěn)高(gāo)此外(wài),傳統抗體的抗原結合位點已進化爲凹形或扁平模式,無法識别具有隐式或隐藏表位的抗原。使用(yòng)抗體的另一個重要問題是,它們可能(néng)會(huì)誘導不必要的免疫原性反應。
納米抗體偶聯策略
小(xiǎo)分子藥物、毒素、酶和(hé)顯像劑等效應基團附着在納米抗體(Nbs)上(shàng)會(huì)産生所謂的Nb偶聯物,這(zhè)可以大(dà)大(dà)擴展納米抗體(Nbs)在癌症治療和(hé)診斷中的适用(yòng)性(圖C)。在這(zhè)種情況下(xià),納米抗體(Nbs)被用(yòng)作(zuò)一種載體,可以以低(dī)系統毒性特異性靶向效應細胞群到(dào)或進入目标部位。Nb偶聯物結合兩者優點的分子,如組織高(gāo)滲透、高(gāo)特異性、強有力的抗腫瘤效果及可成像的性質。
由于其模塊化和(hé)單體性質,納米抗體(Nbs)易于化學修飾和(hé)分子操作(zuò)。利用(yòng)模塊化,通過基因融合可以簡單地構建多價納米抗體(Nbs)、雙特異性納米抗體(Nbs)和(hé)雙異位納米抗體(Nbs),從(cóng)而提高(gāo)親和(hé)力、特異性和(hé)療效。Fc結構域、酶、熒光蛋白(bái)、蛋白(bái)配體和(hé)毒素也(yě)通過基因融合成功地連接到(dào)Nbs上(shàng)。
納米抗體(Nbs)的化學功能(néng)化在傳統上(shàng)最常用(yòng)的是親核半胱氨酸和(hé)賴氨酸。由于裂解素在幾乎所有的蛋白(bái)質表面(包括納米抗體,Nbs)都有很(hěn)高(gāo)的表達率,因此裂解素生物偶聯是一種流行的策略。然而,基于裂解素的生物偶聯方法缺乏控制功能(néng)化的數量和(hé)位置的能(néng)力,導緻Nb偶聯物的混合。此外(wài),随着異質性的增加,如果可尋址溶菌素存在于CDR循環中,納米抗體(Nbs)結合能(néng)力将降低(dī)或喪失。
納米抗體(Nbs)的位點特異性功能(néng)化更可能(néng)通過可尋址的半胱氨酸獲得,因爲它在大(dà)多數蛋白(bái)質序列中豐度低(dī)。通過基因操作(zuò),外(wài)源半胱氨酸可以很(hěn)容易地引入到(dào)羧基端。在大(dà)多數情況下(xià),新引入的半胱氨酸被整合到(dào)納米抗體(Nbs)的c -末端,這(zhè)保證了(le)對(duì)納米抗體(Nbs)抗原識别能(néng)力的最小(xiǎo)幹擾。
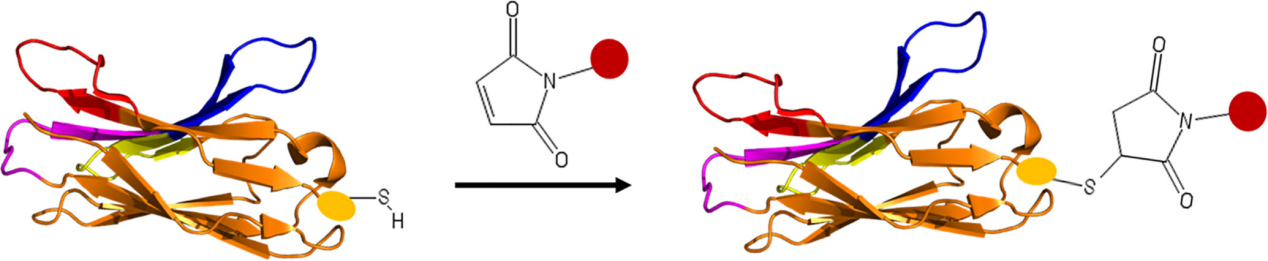
圖:通過工(gōng)程半胱氨酸實現(xiàn)納米體的位點特異性功能(néng)化。半胱氨酸通過基因改造進入納米體。馬來(lái)酰亞胺是應用(yòng)最廣泛的巯基反應性化學基團之一。黃色橢圓形表示外(wài)源半胱氨酸主幹。紅(hóng)色球體表示與馬來(lái)酰亞胺相連的官能(néng)團(如毒素或熒光)。
琥珀抑制是實現(xiàn)納米抗體(Nbs)生物偶聯的另一種技術該方法的亮(liàng)點。将獨特的非天然氨基酸引入蛋白(bái)質序列,這(zhè)些(xiē)氨基酸攜帶活性化學實體,如酮類、疊氮化物和(hé)烯烴,從(cóng)而實現(xiàn)了(le)精細的選擇性。然後,這(zhè)些(xiē)反應基團可以利用(yòng)雙正交偶聯反應将所需的有效載荷特異性地連接到(dào)蛋白(bái)質位點上(shàng)。
治療性納米抗體偶聯物
納米抗體(Nbs)在癌症治療方面具有巨大(dà)的潛力,其中許多都處于臨床試驗階段。在腫瘤學領域,作(zuò)爲拮抗劑的納米抗體(Nbs)已經得到(dào)了(le)廣泛的研究,例如靶向表皮生長因子受體(EGFR)、52人表皮生長因子(HER2)和(hé)肝細胞生長因子受體(HGFR)的納米抗體(Nbs)。這(zhè)些(xiē)拮抗納米抗體(Nbs)可以與腫瘤細胞上(shàng)的細胞外(wài)蛋白(bái)結合,并幹擾其相應的信号通路,從(cóng)而抑制腫瘤細胞的生長和(hé)增殖。然而,由于Fc結構域的缺失,單獨使用(yòng)納米抗體(Nbs)的抗腫瘤效果不如傳統的抗體。理(lǐ)想的抗腫瘤藥物是非常強效和(hé)特異性的,這(zhè)意味着它可能(néng)導緻細胞死亡和(hé)腫瘤消退,而不是抑制癌細胞的增殖,這(zhè)種毒性作(zuò)用(yòng)應嚴格限制在腫瘤部位,避免健康組織。納米抗體(Nbs)與治療藥物的結合有望開(kāi)發出具有更高(gāo)效力的特異性抗癌治療藥物。
納米抗體(Nbs)偶聯物在腫瘤成像中的應用(yòng)
早期診斷是很(hěn)重要的在降低(dī)癌症死亡率。單光子發射計(jì)算(suàn)機斷層顯像(SPECT)、正電子發射計(jì)算(suàn)機斷層顯像(PET)、計(jì)算(suàn)機斷層顯像(CT)和(hé)光學成像等多種技術已被開(kāi)發并應用(yòng)于臨床。由于其體積小(xiǎo)、魯棒性強、穩定性高(gāo)、從(cóng)體内清除快(kuài)等特點,基于納米抗體(Nbs)偶聯物的分子成像技術越來(lái)越受到(dào)關注,這(zhè)使得其能(néng)夠規避基于單克隆抗體的示蹤劑的局限性。
盡管單藥納米抗體(Nbs)已被開(kāi)發爲腫瘤血管生成、代謝(xiè)和(hé)轉移的拮抗劑,但(dàn)将小(xiǎo)分子藥物、毒素、顯像劑和(hé)酶等功能(néng)模塊修飾納米抗體(Nbs)可極大(dà)地拓寬納米抗體(Nbs)在腫瘤治療和(hé)診斷中的應用(yòng)。由于生物偶聯技術的進步,從(cóng)現(xiàn)有的工(gōng)具箱中選擇合适的生物偶聯技術,可以很(hěn)容易地實現(xiàn)納米抗體(Nbs)與其他(tā)模塊的偶聯。然而,由于蛋白(bái)質的脆性和(hé)複雜(zá)性,即使是最可預測的結合技術也(yě)可能(néng)産生意想不到(dào)的蛋白(bái)質結合物。因此,應該指出的是,仔細檢查的綁定屬性合成納米抗體(Nbs)配合進一步的臨床前和(hé)臨床應用(yòng)的先決條件。将納米抗體(Nbs)與毒素結合可能(néng)是結合納米抗體(Nbs)與功能(néng)模塊優勢的最直接的方法。另外(wài),Nb -酶偶聯物已被開(kāi)發用(yòng)于原位激活給藥的前藥。此外(wài),由于其體積小(xiǎo)、擴散快(kuài)、從(cóng)體内洗脫快(kuài),基于納米抗體(Nbs)的成像探針可以在給藥後不久進行高(gāo)對(duì)比度成像。此外(wài),鑒于每種癌症療法都有其自(zì)身的局限性,成功的癌症治療最有可能(néng)通過這(zhè)些(xiē)技術的合理(lǐ)組合來(lái)建立。

 聯系我們
聯系我們





